阿尔法和β碳
目录
阿尔法和β碳
在有机化学中,α碳(Cα)是指连接到官能团(例如羰基)的xxx个碳原子。第二个碳原子称为β碳(Cβ),[1]命名系统按希腊字母顺序继续。该命名法也可以应用于与碳原子相连的氢原子。与α-碳原子相连的氢原子称为α-氢原子,β-碳原子上的氢原子称为β-氢原子,依此类推。这个命名标准可能不符合IUPAC命名法,该命名法鼓励用数字而不是希腊字母来识别碳,但它仍然非常受欢迎,特别是因为它有助于识别碳原子与其他功能的相对位置团体。具有多个官能团的有机分子可能会造成混淆。通常,负责分子名称或类型的官能团是用于碳原子命名的“参考”基团。例如,硝基苯乙烯和苯乙胺的分子非常相似。前者甚至可以归结为后者。然而,硝基苯乙烯的α-碳原子与苯基相邻;在苯乙胺中,这个相同的碳原子是β-碳原子,因为苯乙胺(是胺而不是苯乙烯)从分子的另一端计算其原子。<ulclass=”gallery”>
- 硝基苯乙烯
- 苯乙胺
阿尔法和β碳的例子
蛋白质和氨基酸
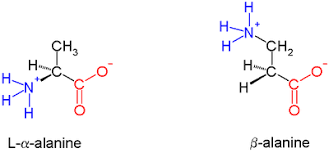
α-碳(α-碳)也是一个适用于蛋白质和氨基酸的术语。它是分子中羰基碳原子之前的主链碳。因此,沿着典型蛋白质的骨架读取会给出一个序列-[N-Cα-羰基C]n-等(当从N到C方向读取时)。α-碳是不同取代基连接到每个不同氨基酸的位置。也就是说,在α-碳链上悬挂的基团赋予了氨基酸多样性。这些基团赋予α-碳对除甘氨酸以外的所有氨基酸的立体特性。因此,α-碳是除甘氨酸以外的所有氨基酸的立体中心。甘氨酸也没有β-碳,而其他所有氨基酸都有。氨基酸的α-碳在蛋白质折叠中很重要。当描述一种由氨基酸链组成的蛋白质时,人们通常将每个氨基酸的位置近似为其α-碳的位置。通常,蛋白质中相邻氨基酸的α-碳相距约3.8埃(380皮米)。
烯醇和烯醇化物
α-碳对于基于烯醇和烯醇化物的羰基化学也很重要。通常,受转化为烯醇化物或烯醇影响的化学转化导致α-碳充当亲核试剂,例如在伯卤代烷存在下被烷基化。一个例外是与甲硅烷基氯化物、溴化物和碘化物反应,其中氧气充当亲核试剂以产生甲硅烷基烯醇醚。