图卡替尼
目录
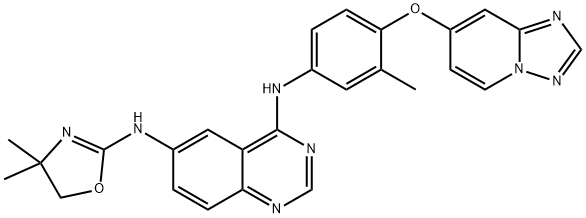
图卡替尼
图卡替尼以商品名 Tukysa 销售,是一种 HER2 小分子抑制剂,用于治疗 HER2 阳性乳腺癌。 它由 Array BioPharma 开发,并授权给 Cascadian Therapeutics(前身为 Oncothyreon,后来成为 Seattle Genetics 的一部分)。
常见的副作用是腹泻、掌跖红肿(手脚灼痛或刺痛不适)、恶心、疲劳、肝毒性(肝损伤)、呕吐、口腔炎(口腔和嘴唇发炎)、食欲下降、腹痛、 头痛、贫血和皮疹。 孕妇或哺乳期妇女不应服用图卡替尼,因为它可能对发育中的胎儿或新生儿造成伤害。
图卡替尼于2020年4月在美国获批用于医疗用途,2020年8月在澳大利亚获批,2021年2月在欧盟获批。
医疗用途
图卡替尼是一种激酶抑制剂,适用于与曲妥珠单抗和卡培他滨联合治疗患有晚期不可切除或转移性 HER2 阳性乳腺癌的成人,包括脑转移患者,这些患者之前接受过一种或多种基于抗 HER2 的治疗方案 在转移环境中。
在欧盟,它与曲妥珠单抗和卡培他滨联合用于治疗至少接受过两种既往抗 HER2 治疗方案的 HER2 阳性局部晚期或转移性乳腺癌成人患者。
临床试验
两项早期临床试验报告了令人鼓舞的结果,这两项试验都可以选择招募患有中枢神经系统 (CNS) 转移的受试者。 HER2CLIMB 是一项关于 tucatinib 联合曲妥珠单抗和卡培他滨治疗经治、不可切除的局部晚期或转移性 HER2阳性乳腺癌患者的随机、双盲、安慰剂对照研究。
历史
2020 年 4 月,美国食品药品监督管理局 (FDA) 批准图卡替尼联合化疗(曲妥珠单抗和卡培他滨)用于治疗无法通过手术切除或已患有晚期 HER2 阳性乳腺癌的成人患者 扩散到身体的其他部位,包括大脑,以及接受过一种或多种先前治疗的人。
FDA 与澳大利亚治疗用品管理局 (TGA)、加拿大卫生部、卫生科学局(HSA,新加坡)和 Swissmedic(SMC,瑞士)合作进行了审查。 这是 FDA、HSA 和 Swissmedic 之间的xxx个 Orbis 项目合作伙伴关系。 截至 2020 年 4 月 17 日,其他机构仍在审查该申请。
图卡替尼是一种激酶抑制剂,这意味着它可以阻断一种酶(激酶)并有助于防止癌细胞生长。 图卡替尼被批准用于成人在转移性环境中服用一种或多种抗 HER2 疗法后的治疗。 FDA 根据 HER2CLIMB 试验 (NCT02614794) 的结果批准了 tucatinib,该试验招募了 612 名患有 HER2 阳性晚期不可切除或转移性乳腺癌且之前接受过曲妥珠单抗、帕妥珠单抗和 ado-trastuzumab emtansine (T-DM1) 治疗的受试者。 既往接受过治疗且脑转移稳定的受试者,以及接受过治疗且正在生长或未接受过治疗的脑转移的受试者均有资格参加临床试验,48% 的入组受试者在试验开始时有脑转移。
受试者接受 tucatinib 300 mg 每天两次加曲妥珠单抗和卡培他滨(tucatinib 组,n=410)或安慰剂加曲妥珠单抗和卡培他滨(对照组,n=202)。 主要终点是无进展生存期(PFS),或肿瘤没有生长的时间,由盲法独立中央审查评估,在最初的 480 名随机患者中进行评估。 接受图卡替尼、曲妥珠单抗和卡培他滨治疗的受试者的中位 PFS 为 7.8 个月(95% CI:7.5、9.6),而接受安慰剂、曲妥珠单抗和卡培他滨治疗的受试者为 5.6 个月(95% CI:4.2、7.1)。 HR 0.54;95% CI:0.42、0.71;p<0.00001)。
基线时有脑转移的受试者的总生存期和 PFS 是关键的次要终点。 接受图卡替尼、曲妥珠单抗和卡培他滨治疗的受试者的中位总生存期为 21.9 个月(95% CI:18.3、31.0),而接受安慰剂、曲妥珠单抗和卡培他滨治疗的受试者为 17.4 个月(95% CI:13.6、19.9)。 HR:0.66;95% CI:0.50、0.87;p=0.00480)。 接受图卡替尼、曲妥珠单抗和卡培他滨治疗的基线时有脑转移的受试者的中位 PFS 为 7.6 个月(95% CI:6.2,9.5),而接受安慰剂、曲妥珠单抗和卡培他滨治疗的受试者为 5.4 个月(95% CI:4.1,5.7) 卡培他滨(HR:0.48;0.34、0.69;p<0.00001)。
FDA 批准了 tucatinib 优先审评、突破性治疗、快速通道和孤儿药物指定的申请。 FDA 批准 Tukysa 给 Seattle Genetics , Inc .